2022-05-11
Минздрав одобрил один из самых дорогих препаратов из перечня «Круга добра»
 | Минздрав зарегистрировал препарат воретиген непарвовек под названием «Лукстурна» компании Novartis. |
2022-05-11
Экопипам в терапии тика при синдроме Туретта
 | Опубликованы результаты исследования нового препарата, блокирующего рецептор допамина-1 (D1), эффективного в снижении тика у детей с синдромом Туретта. |
2022-05-11
Рамил Хабриев: «Система готова к внедрению механизма лекарственного возмещения»
 | Научный руководитель ФГБНУ «Национальный НИИ общественного здоровья имени Н.А.Семашко» о том, как отрасль должна ответить на новые вызовы |
2022-04-27
Российский Фармацевтический Форум им. Н.А. Семашко: главная площадка для встречи фармацевтического рынка обретает новое имя
 | Российский Фармацевтический Форум уже на протяжении 28 лет является главной площадкой для встречи всего фармацевтического рынка России и обсуждения наиболее актуальных и острых вопросов фармацевтической отрасли. Богатая история Форума и те вызовы, с которыми столкнулась национальная система лекарственного обеспечения в настоящее время, обратили взгляд организаторов Форума к историческому опыту построения и формирования уникальной модели национальной системы здравоохранения, построенной выдающимся организатором здравоохранения Николаем Семашко. |
2022-04-27
V Ежегодная Всероссийская научно-практическая конференция с международным участием «Безопасность фармакотерапии: Noli nocere!»
 | Российская медицинская академия непрерывного профессионального образования (ФГБОУ ДПО РМАНПО Минздрава России) приглашает вас принять участие в работе V Ежегодной Всероссийской научно-практической конференции с международным участием «Безопасность фармакотерапии: Noli nocere!». |
2022-04-27
Разработка резидента «Сколково» снижает риски от эмбарго иностранного компонента для вакцины «Спутник V»
 | Компания «Иннова плюс», резидент Фонда «Сколково», разработала отечественный вариант ключевого фермента для создания вакцин без использования иностранного компонента. Разработкой уже заинтересовались — «Р-Фарм», «Биннофарм Групп», «НИЦЭМ им. Н.Ф. Гамалеи». |
2022-04-23
Академик Александр Румянцев: «Осознанное отключение пациентов от медицинской помощи руками медиков и медицинского сообщества является геноцидом»
 | Первый вице-президент Союза медицинского сообщества «Национальная медицинская палата» Александр Румянцев сделал специальное заявление в связи с тем, что компания - официальный дистрибьютор немецкой компании Miltenyi Biotec объявила о намерении приостановить поставку в Россию оборудование и комплектующие материалы для клеточных лечебных технологий, необходимых для лечения детей с онкологическими заболеваниями. |
2022-04-22
Безопасность иксекизумаба у пациентов с псориатическим артритом
 | Оценить безопасность иксекизумаба на группе пациентов с ПсА, принимавших препарат в течение 3 лет. |
2022-04-22
IXORA-PEDS: Иксекизумаб при бляшечном псориазе у детей
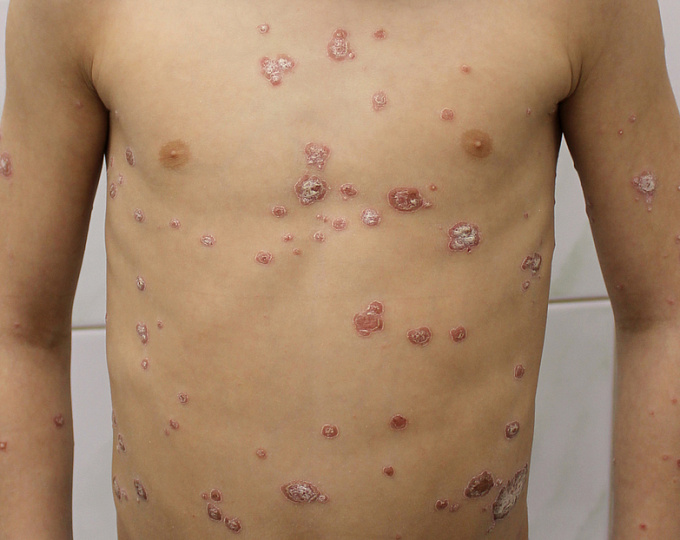 | Участниками многоцентрового рандомизированного исследования были дети и подростки (6-18 лет) с бляшечным псориазом. У всех участников псориаз был умеренный или тяжелый (индекс PASI ≥12; баллы по sPGA ≥3; псориазом поражено ≥10% поверхности тела). |
2022-04-18
В перечень программ ординатуры вошла медицинская микробиология
 | Министерство науки и высшего образования РФ внесло специальность «медицинская микробиология» в перечень специальностей высшего образования – подготовки кадров высшей квалификации по программам ординатуры. |
2022-04-14
Риск случайного повреждения печени у пациентов с ВИЧ, получающих АРВ-терапию
 | Пациенты с моноинфекцией ВИЧ, имеющие повышенный риск поражения печени, должны находиться под тщательным наблюдением врачей в течение всего периода АРВ-терапии. Это также касается и тех людей, которые не имели проблем с печенью до начала приёма антиретровирусных препаратов. |
2022-04-13
27-28 октября 2022 г. состоятся XVI «Санкт-Петербургские дерматологические чтения»
 | Мы приглашаем всех желающих принять участие в XVI «Санкт-Петербургских дерматологических чтениях»:
|
2022-04-13
22-23 сентября 2022 г. состоится конгресс с международным участием XXIV «Давиденковские чтения» (неврология)
 | Мы рады пригласить всех желающих на Конгресс XXIV «Давиденковские чтения», который состоится 22-23 сентября в отеле «Краун Плаза Санкт-Петербург Аэропорт»! |
2022-04-12
Тенектеплаза в лечении острого ишемического инсульта: результаты мета-анализа
 | Работа является систематическим обзором и мета-анализом нерандомизированных исследований, в которых сравнивалась эффективность и безопасность тенектеплазы и алтеплазы у пациентов с острым ишемическим инсультом. |
2022-04-12
18-19 апреля состоится конференция «Актуальные вопросы доклинических и клинических исследований лекарственных средств и клинических испытаний медицинских изделий»
 | IX Всероссийская конференция с международным участием «Актуальные вопросы доклинических и клинических исследований лекарственных средств и клинических испытаний медицинских изделий» |
2022-04-12
Росздравнадзор напомнил рекомендации по эксплуатации подключаемых к интернету медизделий
 | Росздравнадзор напомнил рекомендации по эксплуатации подключаемых к интернету медизделий. Служба разослала в медорганизации информационное письмо. |
2022-04-12
Клиника АО «Медицина» (клиника академика Ройтберга) успешно прошла секретную проверку
 | В АО «Медицина» (клиника академика Ройтберга) подведены итоги программы «Секретный пациент – 2021». Это уже одиннадцатый этап программы, стартовавшей в 2011 году. За 10 лет в программе приняли участие более 300 человек, было получено более 2500 чек-листов. |
2022-04-11
V Ежегодный Всероссийский конгресс, посвящённый актуальным вопросам клинической фармакологии и педиатрии «Лекарство и Дети». 21 апреля 2022 г.
 | Приглашаем Вас принять участие в V Ежегодном Всероссийском Конгрессе «Лекарство и Дети» в формате Онлайн. |
2022-04-11
Что имеем — храним: врачи напоминают о важности регулярной диспансеризации
 | В фундамент современной медицины заложен принцип профилактики. Предотвратить всегда проще, чем вылечить, поэтому врачи по всему миру постоянно говорят о том, как важно вовремя проходить профилактические осмотры. Многие заболевания можно «перехватить» на ранних стадиях, когда гораздо больше шансов остановить их прогрессирование, избежать развития осложнений и получить благоприятный прогноз. В особенности это касается онкологии. |
2022-04-09
Представлен список заболеваний для лечения препаратами OFF-LABEL
 | Минздрав РФ подготовил проект перечня заболеваний, при которых врачи смогут назначать пациентам препараты off-label (вне инструкции). |
2022-04-08
Половина московских специалистов заявила о необходимости усовершенствования фармаконадзора
 | Каждый второй московский специалист (49%) заявил о необходимости усовершенствования фармаконадзора. Только 34% респондентов подают извещения в эту систему при любых побочных реакциях, говорят данные опроса. |
2022-04-08
«Хочу обратиться к вам, уважаемые коллеги, с просьбой ускорить рассмотрение законопроекта. Это вопрос спасения сотен тысяч человеческих жизней», - Премьер-министр РФ Михаил Мишустин
 | Премьер-министр РФ Михаил Мишустин попросил Госдуму ускорить рассмотрение законопроекта о создании единого федерального регистра доноров костного мозга. Сегодня в регистрах доноров в России состоит всего около 170 000 человек, в то время как необходимо не менее 1 миллиона |
2022-04-07
15 научных издательств ограничили сотрудничество с Россией
 | Пятнадцать научных издательств, включая некоторые медицинские, объявили о прекращении продаж и маркетинговых коммуникаций с исследователями из России и Белоруссии в связи с ситуацией на Украине. |
2022-04-05
FDA расширило показания к применению CAR-T-Терапии от GILEAD
 | Управление по контролю за продуктами и лекарствами США (FDA) 1 апреля расширило показания к использованию препарата на основе технологии CAR-T – Yescarta (axicabtagene ciloleucel) – от Gilead Sciences. |














































