Перейти к:
Индивидуализированная профилактика гемофилии А как путь повышения эффективности терапии и оптимизации потребления препаратов на примере октокога альфа и руриоктакога альфа пэгола. Систематический обзор литературы
https://doi.org/10.37489/2588-0519-2021-2-22-29
Аннотация
Цель: обобщение информации об эффективности и потреблении препаратов октоког альфа и руриоктоктог альфа пэгол при стандартной профилактической терапии и профилактической терапии с использованием индивидуализированного подхода у пациентов с гемофилией А на основании опубликованных международных данных. Материалы и методы: был проведён систематический поиск и обзор литературы. Из выявленных в ходе систематического поиска 25 источников было отобрано 7 релевантных источников, описывающих результаты сравнения терапии препаратами октоког альфа и руриоктоког альфа пэгол у взрослых и детей с тяжёлой и среднетяжёлой формами гемофилии А с использованием персонифицированной оценки фармакокинетической кривой на основе программного обеспечения myPKFiT и стандартным режимом дозирования. Проводили объединение и анализ данных об отдельных пациентах во вторично выделяемых подгруппах, в том числе по возрасту, наличию кровотечений, риску кровотечений, связанному с повседневной физической активностью пациентов. Результаты. В наблюдательных исследованиях пересмотр режима дозирования октокога альфа на основании персонифицированной оценки фармакокинетической кривой с использованием myPKFiT привёл к сокращению объёма потребления лекарственных препаратов и/или к повышению эффективности профилактики кровотечений у пациентов с тяжёлой гемофилией А — сокращению среднегодовой частоты кровотечений. В продлённом контролируемом клиническом исследовании применения myPKFiT при терапии руриоктокогом альфа пэгол по сравнению с отсутствием персонификации выявлена тенденция к снижению частоты кровотечений и увеличению среднегодового потребления лекарственного препарата. В исследованиях по оценке одномоментного среза применение myPKFiT приводило к пересмотру режима применения менее чем у четверти пациентов. Заключение. Использование дозирования лекарственных препаратов октоког альфа и руриоктоког альфа пэгол на основе персонифицированной оценки фармакокинетической кривой с применением фармакокинетической популяционной модели приводит к обоснованному корректированию дозы и улучшению исходов.
Ключевые слова
Для цитирования:
Толкушин А.Г., Холовня-Волоскова М.Э., Погудина Н.Л. Индивидуализированная профилактика гемофилии А как путь повышения эффективности терапии и оптимизации потребления препаратов на примере октокога альфа и руриоктакога альфа пэгола. Систематический обзор литературы. Качественная клиническая практика. 2021;(2):22-29. https://doi.org/10.37489/2588-0519-2021-2-22-29
For citation:
Tolkushin A.G., Holownia-Voloskova M.E., Pogudina N.L. Individualized prophylactic treatment of patients with hemophilia A to improve effectiveness and optimize product consumption on the example of octocog alpha and rurioctocog alpha pegol. A systematic literature review. Kachestvennaya Klinicheskaya Praktika = Good Clinical Practice. 2021;(2):22-29. (In Russ.) https://doi.org/10.37489/2588-0519-2021-2-22-29
Введение / Introduction
Гемофилия А — наследственный генетически обусловленный дефицит фактора свёртывания крови VIII — приводит к нарушению свёртывания крови и кровоточивости, которую можно предотвратить посредством заместительной терапии препаратами фактора VIII (FVIII). Тяжёлая форма гемофилии является показанием для проведения постоянной заместительной терапии, также называемой профилактической терапией. [1].
За последнее десятилетие в нашей стране достигнуты существенные улучшения в терапии гемофилии. Благодаря централизованному лекарственному обеспечению пациенты с гемофилией имеют возможность использовать современные высокоэффективные лекарственные препараты [2]. Уровень диагностики и обеспечения FVIII пациентов с гемофилией в России не уступает уровню развитых европейских стран [3]. Снизилась частота кровотечений, возросло качество жизни, трудоспособность, социальная адаптация, увеличился средний возраст пациентов с гемофилией [4]. С 2007 до 2017 гг. средний возраст пациентов увеличился с 29,1 до 37,5 года, количество пациентов с гемофилией, у которых было меньше одного спонтанного кровотечения, увеличилось с 19,2 до 36,3 %; количество работающих пациентов — с 23,3 до 46,3 % [5].
Важным аспектом совершенствования лекарственной помощи людям, живущим с гемофилией, является регистрация новых, ещё более эффективных, удобных в использовании и безопасных лекарственных препаратов. Их рациональное применение и дозирование приводит к повышению приверженности пациентов и улучшению исходов терапии [10].
Одним из широко используемых и эффективных вариантов лечения гемофилии А во взрослой и детской популяциях пациентов является октоког альфа [6]. Октоког альфа является лидером по объёму потребления среди рекомбинантных факторов. На него приходилось 7,5 % затрат бюджета программы ВЗН в 2019 году [7].
В результате модификации и пегилирования молекулы октокога альфа появился препарат руриоктоког альфа пэгол с увеличенным примерно в 1,5 раза временем полувыведения.
Другим направлением развития лекарственной помощи пациентам с гемофилией является персонификация. Подбор дозы и режима применения лекарственных препаратов FVIII зависит от массы тела, но последние исследования и наблюдения показали, что этого уровня персонификации терапии недостаточно. Фармакокинетика FVIII крайне вариабельна в популяции и детерминирована генетически [8]. Индивидуальные генетически обусловленные особенности могут быть оценены с применением методов современной фармакогенетики, секвенирования генома и т. п. [9]. Использование фиксированных доз FVIII при этом может иметь отклонение как в сторону недостаточного остаточного уровня FVIII и, следовательно, повышенного риска спонтанных кровотечений, в том числе внутрисуставных, так и в сторону нерационально завышенного потребления дорогостоящих медикаментов. С целью совершенствования и контроля исходов профилактической терапии и оптимизации экономических затрат может быть использована индивидуализация терапии на основе персонифицированной оценки фармакокинетической кривой [10, 11].
Классическая персонифицированная оценка фармакокинетической кривой сложна для рутинного использования сбора как минимум 10 проб в течение 2—3 дней после одной инъекции препарата, а также потенциально опасного периода «отмывки» от 2 до 7 дней [12, 13]. С целью оценки индивидуальной фармакокинетики FVIII в условиях рутинной клинической практики апробированы параметрические прогностические модели. Для оценки индивидуальной фармакокинетики лекарственных препаратов октоког альфа и руриоктаког альфа пэгол была разработана ковариантная модель, которая с высокой точностью предсказывает фармакокинетические параметры на основании всего двух фармакокинетических проб, а также исходных персональных характеристик пациента [14]. Эта модель легла в основу разработки интерактивного инструмента оценки индивидуальных особенностей фармакокинетики этих препаратов — myPKFiT. Применение этого инструмента не требует обязательного пересмотра дозирования, предоставляя дополнительную клиническую информацию для практикующих специалистов. На территории России программное обеспечение myPKFiT на основе веб-приложения зарегистрировано в качестве изделия медицинского применения (Регистрационное удостоверение от 12 марта 2020 года № РЗН 2017/6449) и доступно для использования без взимания платы.
Продолжает оставаться открытым вопрос о влиянии внедрения персонифицированной оценки фармакокинетической кривой на уровень потребления лекарственных препаратов и, следовательно, экономические затраты.
Целью настоящей работы являлось обобщение информации из литературных источников об эффективности профилактической терапии при использовании myPKFit и оценка влияния внедрения myPKFit на объём потребления препаратов октоког альфа и руриоктоког альфа пэгол для профилактической терапии гемофилии А.
Материалы и методы / Material and methods
Для оценки эффективности и изменения объёма потребления в результате индивидуализации подбора дозы и режима применения октокога альфа и руриоктокога альфа пэгол проведён систематический поиск в электронной базе данных PubMed и научной электронной библиотеке eLibrary, который был дополнен поиском в открытом Интернете (Google Scholar, Яндекс). Комбинации ключевых поисковых фраз включали: myPKFit, Advate, octocog, Adynovate, rurioctocog, pharmacokinetic tailoring.
С целью постановки задачи исследования и отбора релевантных публикаций использовали подход PICO — population, intervention, comparator, outcome (популяция пациентов, вмешательство, альтернатива сравнения, клинический исход) [15]. Выявленные источники информации оценивали по следующим критериям отбора:
Популяция пациентов: пациенты с гемофилией А, преимущественно с тяжёлой формой заболевания, взрослые и дети, получающие предшествующую терапию.
Вмешательство: индивидуализированный выбор режима дозирования октокога альфа или руриоктокога альфа пэгол на основании фармакокинетического тестирования с применением программного обеспечения myPKFiT.
Сравниваемая альтернатива: стандартный режим дозирования без персонифицированной оценки фармакокинетической кривой.
Критерии клинической эффективности: средние курсовые дозы лекарственных препаратов, среднегодовая частота кровотечений.
Для оценки объёмов потребления были отобраны исследования, в которых были представлены индивидуальные сведения о дозах до и после фармакокинетической коррекции.
В условиях отсутствия концентрированных данных о влиянии персонифицированной оценки фармакокинетической кривой на изменение дозирования лекарственных препаратов анализировали имеющуюся практику персонифицированной оценки фармакокинетической кривой, представленную в литературе.
С целью гармонизации и дальнейшего анализа данных о режимах применения рассчитывали среднесуточную кратность (частоту) — количество доз в сутки в среднем. В частности, для режима «три раза в неделю» среднесуточная частота составляла 0,43, для режима «каждые 48 часов» — 0,50. Для всех пациентов определяли годовое потребление лекарственного препарата в количестве международных единиц (МЕ).
Результаты и обсуждение / Results and discussion
В результате систематического поиска и отбора исследований выделено 7 релевантных источников (табл. 1). Из них 6 исследований по октокогу альфа и одно исследование по руриоктокогу альфа пэгол (Chowdary P [22]). Данное исследование — единственное из отобранных, в котором использован дизайн интервенционного проспективного контролируемого исследования, являющегося продолжением рандомизированных клинических исследований руриоктокога альфа пэгола третьей фазы, остальные шесть имели дизайн обсервационного наблюдения и описания серий случаев с небольшим количеством пациентов. Из них выявлено всего 5 источников, в которых представлены индивидуальные деперсонифицированные данные о конкретных пациентах с гемофилией А, получающих октоког альфа и прошедших фармакокинетический скрининг с применением инструмента myPKFiT.
Таблица 1
Характеристика отобранных для анализа клинических исследований
Table 1
Characteristics of the selected clinical researches
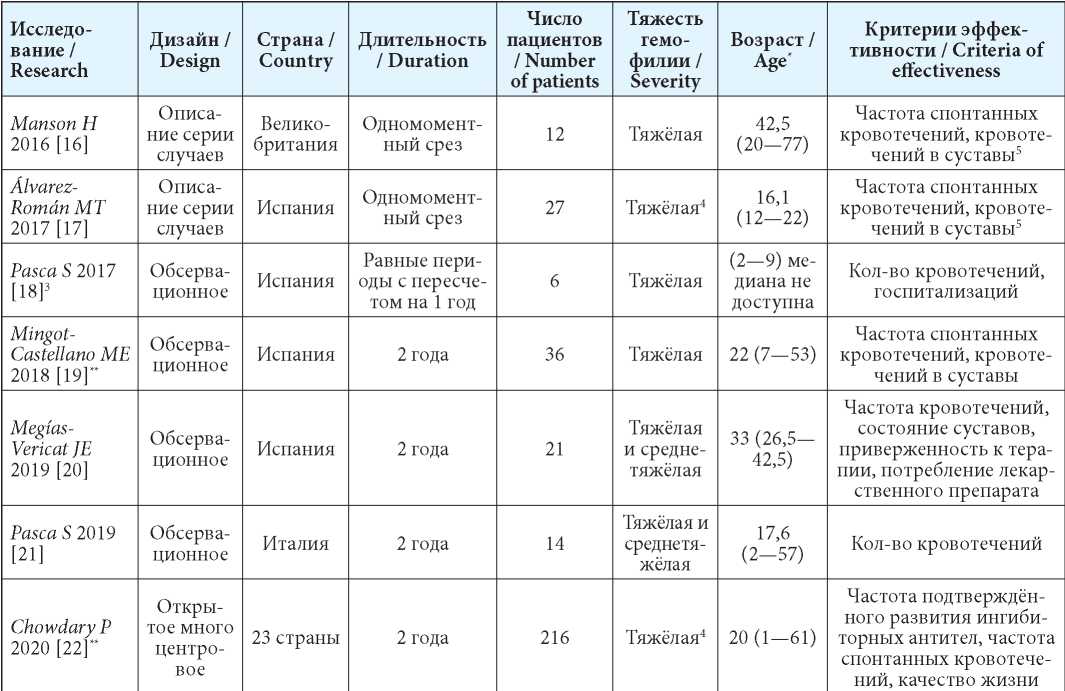
Примечания: * — Медиана (минимум-максимум); ** — не представлены данные по отдельным пациентам; 3 — не представлены обобщенные данные; 4 — часть пациентов получали терапию по требованию до включения в исследование; 5 — не представлены данные по эффективности, представлены данные о клинических исходах, наблюдаемые до проведения фармакокинетического скрининга.
Notes: * — Median (minimum-maximum); ** — data on individual patients are not presented; 3 — generalized data are not presented; 4 — some patients received on-demand therapy before inclusion in the study; 5 — efficacy data are not presented, data on clinical outcomes observed before pharmacokinetic screening are presented.
В качестве основного показателя эффективности в рассмотренных клинических исследованиях была использована частота кровотечений. В некоторых исследованиях дополнительно представлены данные по частоте кровотечений в суставы. В двух исследованиях, представляющих по дизайну одномоментный срез (Manson H [16] и Álvarez-Román MT [17]), данные об эффективности не были представлены, сведения о частоте кровотечений представлены для пациентов до фармакокинетического скрининга. Эти исследования были пригодны для оценки влияния фармакокинетического мониторинга с использованием инструмента myPKFiT на режим применения и объём потребления лекарственного препарата.
В большинстве исследований была рассмотрена смешанная по возрасту популяция пациентов. В одно исследовании (Pasca S [18]) были включены только дети до 9 лет. В исследованиях Álvarez-Román MT [17] и Pasca S [21] медиана возраста пациентов соответствовала подростковой популяции пациентов.
Четыре исследования обсервационного дизайна имели исторический контроль. В них представлены результаты (частота клинических исходов, режим дозирования) в течение одного года до персонифицированной оценки фармакокинетической кривой и одного года после.
В исследовании Manson H [16] из 12 пациентов, прошедших фармакокинетический скрининг, у трёх пациентов при пересмотре дозы и частоты приёма на фоне стабильных показателей кровотечений и показателя по шкале оценки состояния суставов при гемофилии (HJHS) была снижена доза, в то время как остальные 9 пациентов не нуждались в изменении назначенной им профилактики с использование октокога альфа.
Álvarez-Román MT соавт. [17] тоже провели фармакокинетический скрининг, в результате которого из 27 включённых пациентов всего у 7 пациентов был изменён режим дозирования (из них 2 случая снижения дозы, 2 случая учащения режима и 2 случая увеличения одной из трёх недельных доз — пятничной дозы), в двух случаях потребовалась беседа с пациентом или его родителями по планированию физических активностей, и в 1 случае, у единственного пациента из выборки, у которого не была начата профилактика (только терапия по требованию) при наличии множественных кровотечений, профилактика была инициирована.
Обобщая результаты этих двух исследований, можно заключить, что в результате уточнения индивидуальных фармакокинетических особенностей пересмотр режима применения требуется менее чем у 25 % пациентов; в зависимости от исходного уровня дозирования может потребоваться как повышение, так и снижение объёма потребления лекарственного препарата.
Результаты трёх обсервационных исследований, в которых были представлены обобщённые сведения об эффективности и потреблении лекарственного препарата, в целом согласуются между собой (табл. 2). В результате персонифицированной оценки фармакокинетической кривой наблюдается общая тенденция как к снижению частоты кровотечений, так и к снижению объёма потребления октокога альфа. Причём, если в исследовании Mingot Castellano ME [19] выявлено повышение клинической эффективности (-2,2±1,3, P=0,018 для частоты кровотечений и 1,9±1,2, P=0,012 для частоты кровотечений в суставы) при незначительном снижении объёма потребления, то в исследовании Megías-Vericat JE [20] более выражена тенденция к снижению потребления (Р=0,48), чем к улучшению клинических исходов (Р=0,79 и 0,82 для кровотечений и кровотечений в суставы соответственно).
Таблица 2
Обобщённые результаты обсервационных исследований по критериям «частота кровотечений в год», «частота кровотечений в суставы в год» и среднегодовая доза
Table 2
Consolidated results of observational studies on the criteria «bleeding rate per year», «joint bleeding rate per year» and the average annual dose

Исследования Pasca S как в 2019 г. [21], так и в 2017 г. [18], были сфокусированы на индивидуальных характеристиках и последующей экономической оценке. В результате персонифицированной оценки фармакокинетической кривой в этих исследованиях объём потребления лекарственного препарата в год был снижен у 81,8 % пациентов. Последующая экономическая оценка, проведённая для каждого из двенадцати пациентов с тяжёлой формой гемофилии А, включённых в этот анализ, в котором сравнили стандартную и ФК-адаптированную профилактику, показала, что оптимизированное лечение может привести к среднегодовой экономии в размере 20 525 евро (-15,8 %). Аналогичная оценка, проведённая в 2017 году для пациентов с гемофилией А в возрасте младше 9 лет, показала экономию в размере 54 797,40 евро (-10,67 %). В результате фармакокинетической оценки недельная частота инфузий была снижена у одного пациента, в то время как у трёх детей она была несколько увеличена. Плановое наблюдение выявило полную приверженность к лечению, уменьшение кровотечений при использовании индивидуализированного режима и общее улучшение качества жизни.
В статье Зозуля Н.И. [10] детально описаны современные тенденции в сфере фармакокинетической персонификации терапии у пациентов с гемофилией, а также приведён один клинический случай, представленный в рамках конференции Испанского общества по тромбозу и гемостазу в 2015 году. У этого пациента в результате персонифицированной оценки фармакокинетической кривой был пересмотрен режим применения с целью сокращения риска кровотечений с увеличением интервала между введениями препарата, но увеличением общей дозы препарата (с 22 200 до 28 270 МЕ в месяц) и уровня комплаентности. Представленных в источнике данных о клиническом случае было недостаточно для включения в обобщённый анализ.
Единственное отобранное для обзора клиническое исследование по руриоктокогу альфа пэгол имело контролируемый проспективный дизайн. Среднегодовая частота кровотечений составила 1,20 (0,92—1,56) для 186 пациентов, получавших профилактику в фиксированной дозе 2 раза в неделю, и 0,96 (0,54—1,71) для 25 пациентов, получавших фармакокинетически адаптированную профилактику. Средняя курсовая доза составила 4564,0 (988,6) и 5644,4 (2228,9) МЕ/кг в год для фиксированного и фармакокинетически адаптированного режима дозирования.
В двух обсервационных исследованиях (Pasca S [21] и Megías-Vericat JE [20]) были представлены данные по конкретным пациентам, которые подвергали обобщённому анализу. После исключения пациентов, которые до фармакокинетической персонификации получали терапию по требованию (6 человек), а также пациентов, которым терапия не была пересмотрена в результате оценки индивидуальной фармакокинетики (11 человек), общее количество пациентов, включённых в анализ, составило 18 человек. Средний возраст составил 21 (±15) год. Средняя недельная доза октокога альфа сократилась с 83,8±28,2 МЕ/кг/сут до 72,8±18,8 МЕ/кг/сут (p=0,0215). Средняя частота кровотечений сократилась с 1,4±1,7 до 0,9±1,3 (p=0,0952). Таким образом, в результате фармакокинетической персонификации существенно снижались средние объёмы потребления, а также имелась тенденция к улучшению клинического исхода — среднегодовой частоты кровотечений (рис. 2).
Причём, наблюдали преимущественно снижение дозы, однако встречались и случаи повышения дозы (рис. 3).
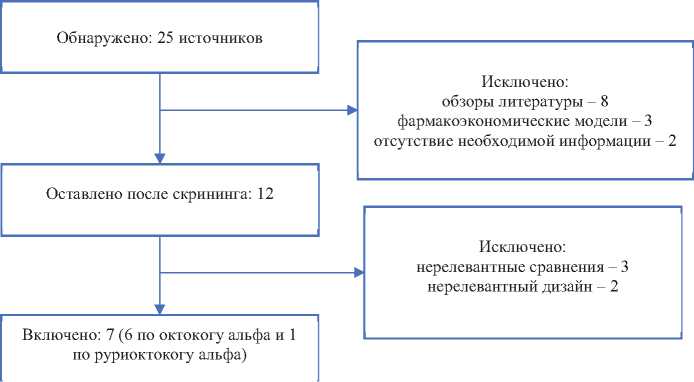
Рис. 1. Потоковая диаграмма поиска и отбора публикаций для включения в анализ
Figure 1. Flow chart of the search and selection of publications for inclusion in the analysis
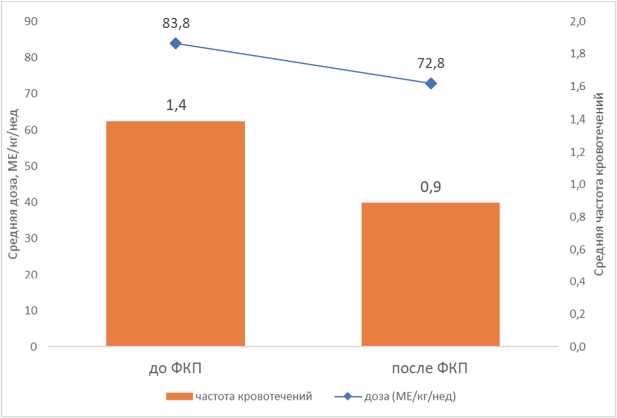
Рис. 2. Результаты обобщённого анализа
Figure 2. Results of consolidated analysis
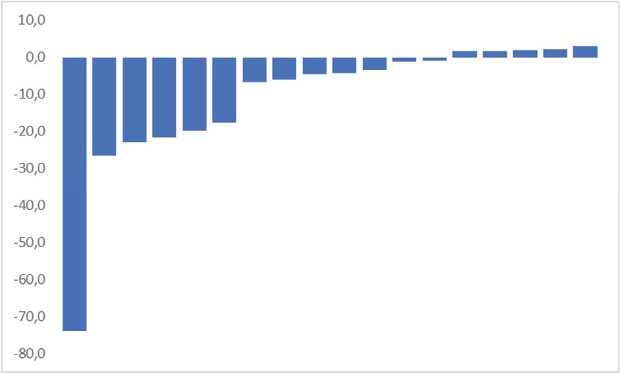
Рис. 3. Индивидуальные изменения дозы (МЕ/кг/нед) у включённых в анализ пациентов
Figure 3. Individual dose changes (IU/kg/week) in the patients included in the analysis
Заключение / Conclusion
В зависимости от дизайна исследований, используемого стандартного режима дозирования, применение ФК-адаптированного подхода приводило либо к сокращению потребления октокога альфа при равной высокой эффективности, либо к повышению эффективности профилактики (предотвращению кровотечений) при сопоставимом уровне потребления лекарственного препарата в год. При этом коррекция режима применения октокога альфа требуется лишь части пациентам с неудовлетворительным контролем уровня FVIII, что может привести к появлению или учащению кровотечений, а также пациентам, которые ведут активный образ жизни, включающий изменение обстоятельств и уровня активности. Указанные заключения в ещё большей степени соответствуют характеристикам руриоктокога альфа пэгол, позволяющего ещё больше увеличить интервалы между инъекциями.
Принимая во внимание разнородность данных, наличие как повышения, так и снижения дозы октокога альфа в популяции в результате персонифицированной фармакокинетической оценки, для уточнения её влияния на реальное потребление лекарственных препаратов в российских условиях актуальным представляется сбор и анализ сведений о применении инструмента myPKFiT на территории Российской Федерации.
Список литературы
1. Клинические рекомендации по диагностике и лечению гемофилии.Коллектив авторов под руководством академика В.Г. Савченко. Рекомендации утверждены на IV Конгрессе гематологов России (апрель 2018). Доступно по: https://npngo.ru/uploads/media_document/284/6abc18ec-97fe-468f-9235-8c0084874289.pdf Ссылка активна на 22.06.2021.
2. Толкушин А.Г., Фёдоров А.А., Жулёв Ю.А., Погудина Н.Л., Ермолаева Т.Н. Направления развития программы лекарственного обеспечения высокозатратных нозологий. Здравоохранение Российской Федерации. 2019;63(5):237-244. doi: 10.18821/0044-197X-2019-63-5-237-244
3. Report on the Annual Global Survey 2019 is published by the World Federation of Hemophilia. [cited 2021 Jun 22] Available from: https://elearning.wf.org/resource/report-on-the-annual-global-survey-2019/
4. Воробьев П.А., Краснова Л.С., Воробьев А.П., Зыкова А.Б., Жулев Ю.А., Зозуля Н.И. Эпидемиология, экономика и качество жизни больных с гемофилией в России в 2007-2017 гг.: результаты применения стандартизации в терапии. Проблемы стандартизации в здравоохранении. 2018;(9-10):15-34. doi: 10.26347/1607-2502201809-10026-034
5. Гемофилия. Качество жизни. 2007-2017. [интернет]. Доступ по: https://hemophilia.ru/library/inf-present/800-gemofliya-kachestvo-zhizni-2007-2017.html Ссылка активна на 22.06.2021.
6. Keating GM, Dhillon S. Octocog alfa (Advate®): a guide to its use in hemophilia A. BioDrugs. 2012 Aug 1;26(4):269-73. doi: 10.1007/BF03261885.
7. DSM Group: Доля российских компаний в структуре закупок в рамках программы ЛЛО сократилась. [DSM Group: Dolya rossijskih kompanij v strukture zakupok v ramkah programmy LLO sokratilas’. (In Russ).] Доступно по: https://pharmvestnik.ru/content/news/DSM-Group-Dolya-rossiiskihkompanii-v-strukture-zakupok-v-ramkah-programmy-LLO-sokratilas.html Ссылка активна на 22.06.2021.
8. Garcia-Martínez I, Borràs N, Martorell M, Parra R, Altisent C, Ramírez L, Álvarez-Román MT, Nuñez R, Megias-Vericat JE, Corrales I, Alonso S, Vidal F. Common Genetic Variants in ABO and CLEC4M Modulate the Pharmacokinetics of Recombinant FVIII in Severe Hemophilia A Patients. Tromb Haemost. 2020 Oct;120(10):1395-1406. doi: 10.1055/s-0040-1714214.
9. Кукес В.Г. Клиническая фармакогенетика / Сычев Д.А., Раменская Г.В., Игнатьев И.В., Кукес В.Г. — Москва: ГЭОТАР-Медиа, 2007. — 248 с. URL: https://www.rosmedlib.ru/book/ISBN9785970404584.html Ссылка активна на 22.06.2021.
10. Зозуля Н.И., Румянцев А.Г. Индивидуализированный подход к профилактической терапии пациентов с тяжелой гемофилией а. Российский журнал детской гематологии и онкологии (РЖДГиО). 2018;5(3):89-94. doi: 10.17650/2311-1267-2018-5-3-89-94
11. Ar MC, Vaide I, Berntorp E, Björkman S. Methods for individualising factor VIII dosing in prophylaxis. Eur J Haematol Suppl. 2014 Aug;76:16-20. doi: 10.1111/ejh.12370.
12. McEneny-King A, Iorio A, Foster G, Edginton AN. Te use of pharmacokinetics in dose individualization of factor VIII in the treatment of hemophilia A. Expert Opin Drug Metab Toxicol. 2016;12(11):1313-1321. DOI: 10.1080/17425255.2016.1214711.
13. Yu JK, Iorio A, Edginton AN; WAPPS co-investigators. Using pharmacokinetics for tailoring prophylaxis in people with hemophilia switching between clotting factor products: A scoping review. Res Pract Tromb Haemost. 2019 May 20;3(3):528-541. doi: 10.1002/rth2.12204. Erratum in: Res Pract Tromb Haemost. 2019 Sep 16;3(4):771. PMID: 31294337; PMCID: PMC6611373.
14. Blanchette V, Zunino L, Grassmann V, Barnes C, Carcao M, Curtain J, Jackson SC, Khoo L, Komrska V, Lillicrap D, Morfni M, Romanova G, Stephens D, Zapotocka E, Rand ML, Blatny J. A practical, one-clinic visit protocol for pharmacokinetic profle generation with the ADVATE®myPKFiT® dosing tool in severe hemophilia A subjects. Tromb Haemost. 2021 Jan 27. doi: 10.1055/a-1376-0970.
15. Richardson WS, Wilson MC, Nishikawa J, Hayward RS. Te wellbuilt clinical question: a key to evidence-based decisions. ACP J Club. 1995 Dec;123(3):A12—3
16. Manson H, Benson G, McAfee C. Belfast Adult’s experience of using a pharmacokinetic personalised treatment tool to maximise factor replacement. Haemophilia. 2016;22(Suppl. 4):126-127.
17. Álvarez-Román MT, Fernandez-Bello I, de la Corte-Rodríguez H, Hernández-Moreno AL, Martín-Salces M, Butta-Coll N, Rivas-Pollmar MI, Rivas-Muñoz S, Jiménez-Yuste V. Experience of tailoring prophylaxis using factor VIII pharmacokinetic parameters estimated with myPKFiT® in patients with severe haemophilia A without inhibitors. Haemophilia. 2017 Jan; 23(1):e50-e54. doi: 10.1111/hae.13141.
18. Pasca S, Milan M, Sarolo L, Zanon E. PK-driven prophylaxis versus standard prophylaxis: When a tailored treatment may be a real and achievable cost-saving approach in children with severe hemophilia A. Tromb Res. 2017 Sep;157:58-63. doi: 10.1016/j.thromres.2017.07.003.
19. Mingot-Castellano ME, Parra R, Núñez R, Martorell M. Improvement in clinical outcomes and replacement factor VIII use in patients with haemophilia A afer factor VIII pharmacokinetic-guided prophylaxis based on Bayesian models with myPKFiT®. Haemophilia. 2018 Sep;24(5):e338-e343. doi: 10.1111/hae.13540.
20. Megías-Vericat JE, Bonanad S, Haya S, Cid AR, Marqués MR, Monte E, Pérez-Alenda S, Bosch P, Querol F, Poveda JL. Bayesian pharmacokineticguided prophylaxis with recombinant factor VIII in severe or moderate haemophilia A. Tromb Res. 2019 Feb;174:151-162. doi: 10.1016/j.thromres.2018.12.027.
21. Pasca S, Zanon E. Savings without changing: How to use the MyPKft® device to improve treatment strategies in a cohort of patients with haemophilia A. Tromb Res. 2019 Nov;183:1-3. doi: 10.1016/j.thromres.2019.08.022.
22. Chowdary P, Mullins ES, Konkle BA, McGuinn C, Park YS, Stasyshyn O, Zulfkar B, Engl W, Tangada S. Long-term safety and efcacy results from the phase 3b, open-label, multicentre Continuation study of rurioctocog alfa pegol for prophylaxis in previously treated patients with severe haemophilia A. Haemophilia. 2020 Jul;26(4):e168-e178. doi: 10.1111/hae.14052.
Об авторах
А. Г. ТолкушинРоссия
Толкушин Александр Геннадьевич, к. ф. н., ведущий специалист отдела оценки медицинских технологий. SPIN-код: 7706-3809
Москва
М. Э. Холовня-Волоскова
Россия
Холовня-Волоскова Мальвина Эва Альбертовна, заведующая отделом оценки медицинских технологий. SPIN-код: 6435-2624
Москва
Н. Л. Погудина
Россия
Погудина Наталья Леонидовна, генеральный директор
Москва
Рецензия
Для цитирования:
Толкушин А.Г., Холовня-Волоскова М.Э., Погудина Н.Л. Индивидуализированная профилактика гемофилии А как путь повышения эффективности терапии и оптимизации потребления препаратов на примере октокога альфа и руриоктакога альфа пэгола. Систематический обзор литературы. Качественная клиническая практика. 2021;(2):22-29. https://doi.org/10.37489/2588-0519-2021-2-22-29
For citation:
Tolkushin A.G., Holownia-Voloskova M.E., Pogudina N.L. Individualized prophylactic treatment of patients with hemophilia A to improve effectiveness and optimize product consumption on the example of octocog alpha and rurioctocog alpha pegol. A systematic literature review. Kachestvennaya Klinicheskaya Praktika = Good Clinical Practice. 2021;(2):22-29. (In Russ.) https://doi.org/10.37489/2588-0519-2021-2-22-29

















































